NOMENCLATURA
Introducción. La Nomenclatura es el idioma de la Química, lo que hace que esta sea muy importante ya que esta permite facilitar la identificación de la estructura de un compuesto por parte del lector; es por ello que se hace énfasis en los nombres sistemáticos, que se ajustan a las reglas de nomenclatura aceptadas internacionalmente, las cuales han evolucionado por cerca de cien años, son el resultado del estudio cuidadoso y el acuerdo previo entre los miembros de una organización de químicos denominada I.U.P.A.C (unión internacional de Química pura y aplicada).
El nombre sistemático de un compuesto orgánico consta de tres partes:
PREFIJO 2º PREFIJO 1º RAIZ SUFIJO 1º SUFIJO 2º
- La raíz es la unidad básica del nombre, se relaciona con la cadena principal del compuesto y es esencial en todo nombre.
- Los prefijos son accidentales, pueden ser o no parte constitutiva del nombre de un compuesto dependiendo de la estructura.
- Los accidentes estructurales se designa mediante prefijos primarios y/o secundarios, el secundario comprende los radicales y las funciones secundarias y el primero se refiere a la naturaleza de la raíz o secuencia carbonada principal.
- Por último, se tienen los sufijos, que son también esenciales en el nombre, los cuales se clasifican en primarios y secundarios; los sufijos primarios se relacionan con el tipo de enlace entre los átomos de carbono de la cadena principal y los sufijos secundarios con la función principal.
Importante.
La secuencia principal debe ser la cadena continua más extensa de átomos de carbono que cumpla el siguiente orden de prioridades, incluyendo:
a. El mayor número de veces la función principal
b. El mayor número de instauraciones con predomino del enlace doble sobre el triple.
c. El mayor número de otros grupos funcionales y sustituyentes en general.




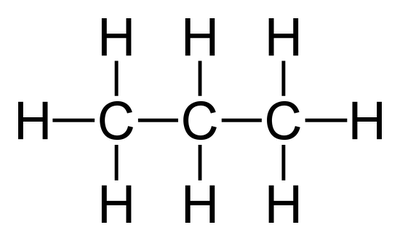 Propano
Propano

